zur Startseite zu Tetrazin-Synthesen
"Synthese, Reaktionsverhalten und Analytik der 1,2,4,5-Tetrazine"
Frank Thalmann , Dissertation 1991, Universität Halle
"Verfahren zur Herstellung von 3-substituierten 6-Alkoxy-1,2,4,5-tetrazinen", DDR-Wirtschaftspatent C07D
295 837 (1990); Just, Manfred; Thalmann, Frank
Die Reaktionen von Mercapto-tetrazinen und Halogen-tetrazinen mit primären
und sekundären Aminen sind vielfältig untersucht. Hier stand das wenig
beschriebene Problem im Vordergrund substituierte Amine ohne den Umweg über die
unsubstituierten Verbindungen herzustellen.
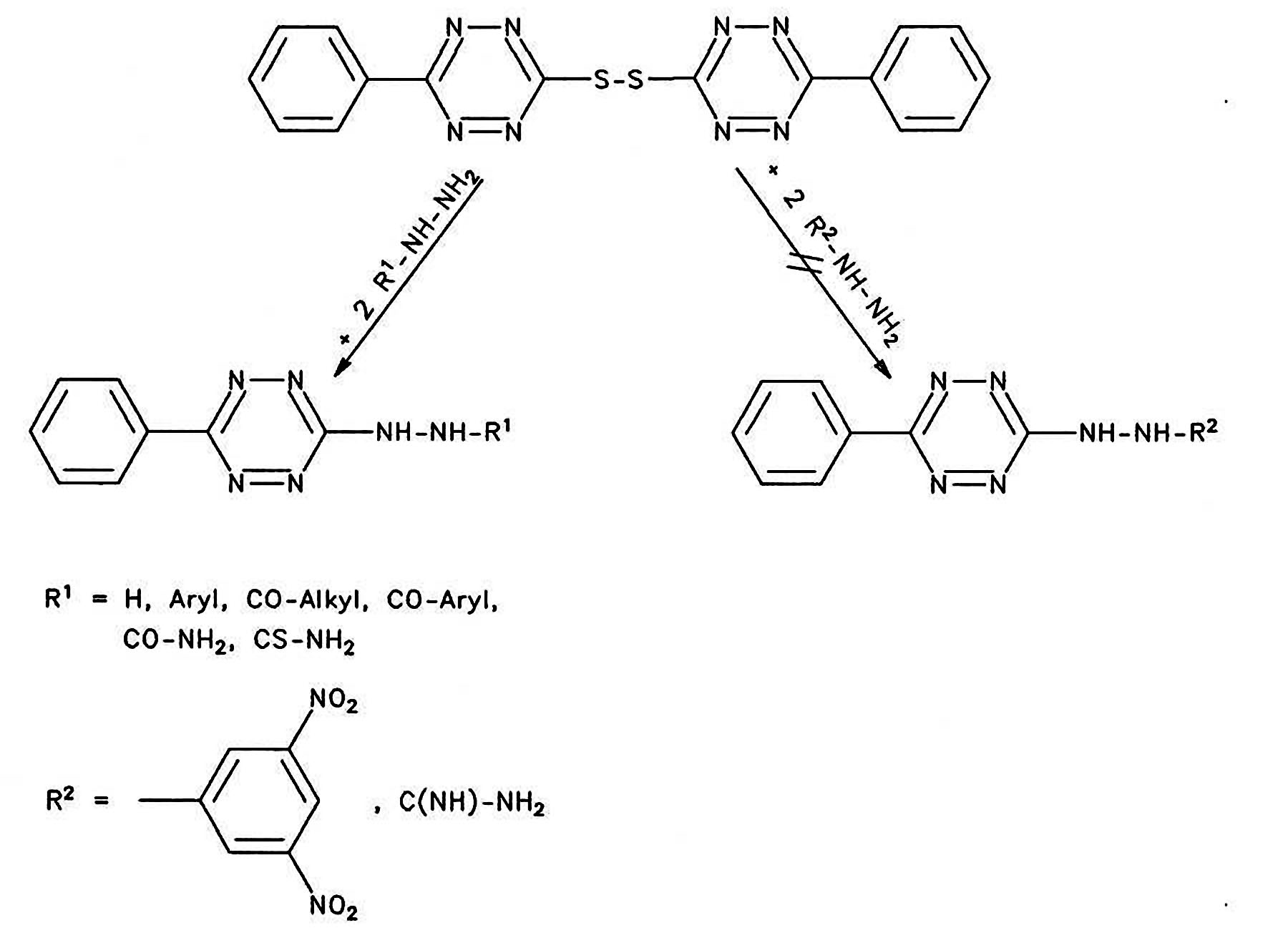
Dabei konnte gezeigt werden, dass Amide
und Harnstoffe nicht direkt reagieren.
Das Amino-phenyl-tetrazin kann in 56%iger Ausbeute und das
Hydrazino-phenyl-tetrazin in 92%iger Ausbeute isoliert werden. (Vorschrift
4)

Substituierte Hydrazine, Acylhydrazide, Semicarbazide, Thiosemicarbazide reagieren mit brauchbaren Ausbeuten zu den Zielverbindungen. Nur das Dinitrophenylhydrazin war nicht umsetzbar. Das Aminoguanidin reagiert zu einem kaum trennbaren Substanzgemisch. (Vorschrift 4)
| R1 | Fp. (°C) | Ausbeute (%) |
| -H | 174-176 | 92 |
| -CO-CH3 | 222 | 77 |
| -CO-C6H5 | 216-218 | 80 |
| -CO-NH2 | 190-192 | 41 |
| -CS-NH2 | >32 | 11 |
Beim Einsatz vom Reaktionspartnern mit konkurrierenden Funktionellen-Gruppen bilden sich, wie erwartet, keine einheitlichen Produkte. Amino- und Hydroxylgruppen unterscheiden sich nur wenig in der Reaktivität, wie am Beispiel von Hydroxylamin und Ethanolamin gezeigt werden konnte. (Vorschrift 4)
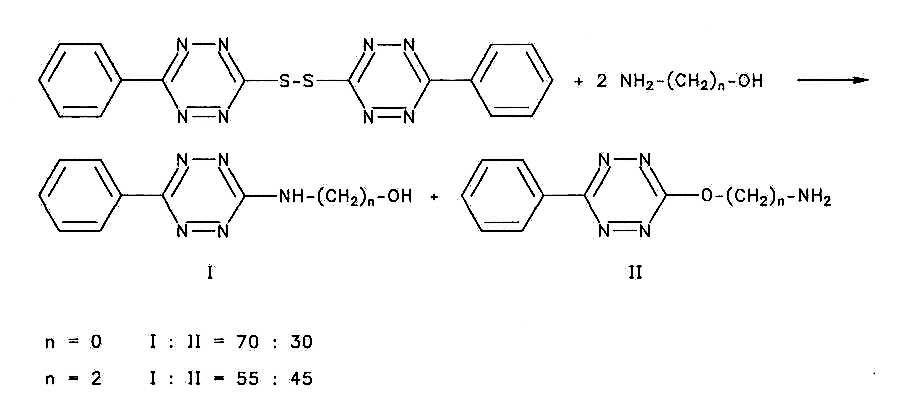
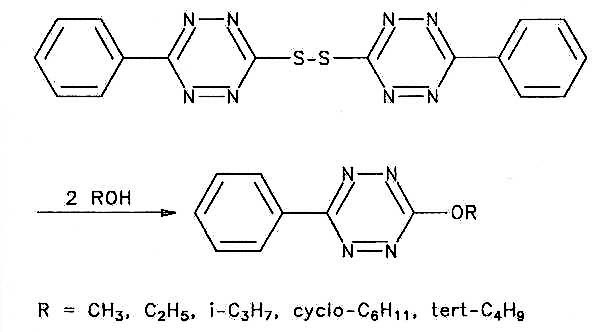
Dazu wurde das Mercapto-Tetrazin mit einem zehnfachen Überschuss des Alkohols in Gegenwart von Pyridin umgesetzt. Primäre, sekundäre und tertiäre reagierten in gleicher Weise. Die Reaktionszeiten mussten angepasst werden. (Vorschrift 5)
| R | Fp. (°C) | Ausbeute (%) |
| Methyl | 85-87 | 89 |
| Ethyl | 102 | 91 |
| i-Propy | 95-96 | 82 |
| Cyclohexyl | 93-94 | 85 |
| Benzyl | 107-108 | 70 |
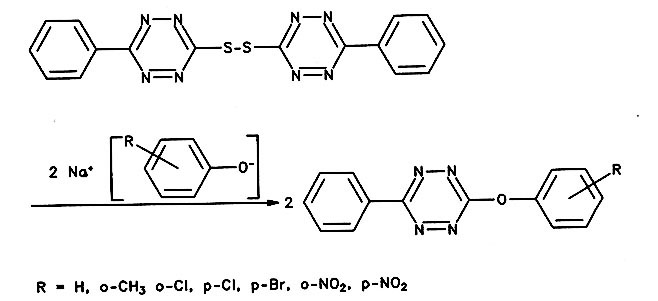
Über Tetrazin-phenol-ether wurde bisher wenig berichtet. Das Mercapto-tetrazin reagiert in wasserfreiem Benzen rasch mit den entsprechenden Phenolaten. Die Umsetzung ist weitgehendst unabhängig von den Substituenten am Phenol. (Vorschrift 5)
Reaktion von Hydrazino-1,2,4,5-tetrazinen mit Carbonylverbindungen
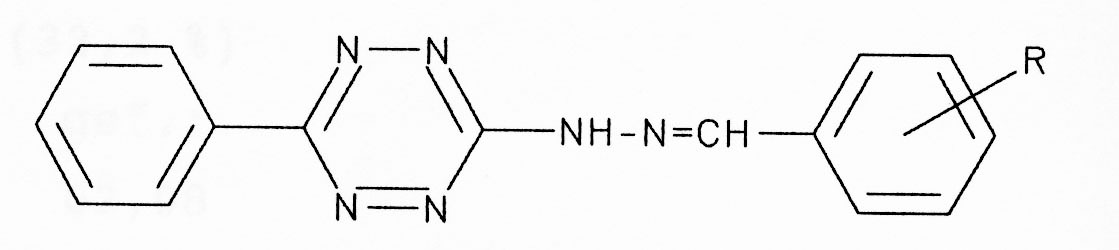 Das Reaktionsverhalten des 3-Hydrazino-6-phenyl-1,2,4,5-tetrazins
unterscheidet sich nicht von den üblichen Hydrazin-Reaktionen. Das zeigen einige
ausgewählte Synthesen.
Das Reaktionsverhalten des 3-Hydrazino-6-phenyl-1,2,4,5-tetrazins
unterscheidet sich nicht von den üblichen Hydrazin-Reaktionen. Das zeigen einige
ausgewählte Synthesen.
| R | Fp.: (°C) | Ausbeute (%) |
| 4-Methoxy | 205-206 | 21 |
| 2-Hydroxy | 265-267 | 32 |
| 4-Dimethylamino | 227-229 | 57 |
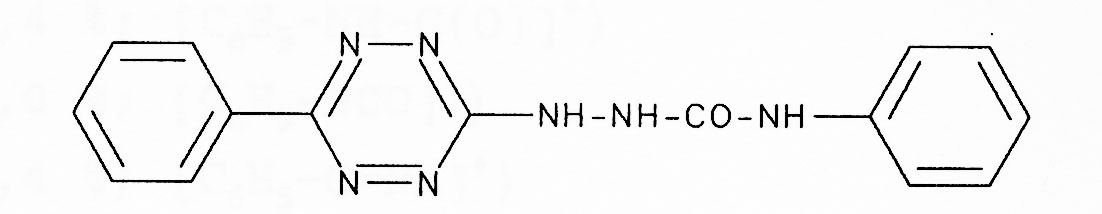
Reaktion von Hydrazino-1,2,4,5-tetrazinen mit Isocyanaten und Isothiocyanaten
 Das
1-(6-Phenyl-1,2,4,5-tetrazin-3-yl)-4-phenyl-semicarbazid wird mit
Phenylisocyanat aus dem Hydrazino-tetrazin in Essigsäureethylester erhalten.
Das
1-(6-Phenyl-1,2,4,5-tetrazin-3-yl)-4-phenyl-semicarbazid wird mit
Phenylisocyanat aus dem Hydrazino-tetrazin in Essigsäureethylester erhalten.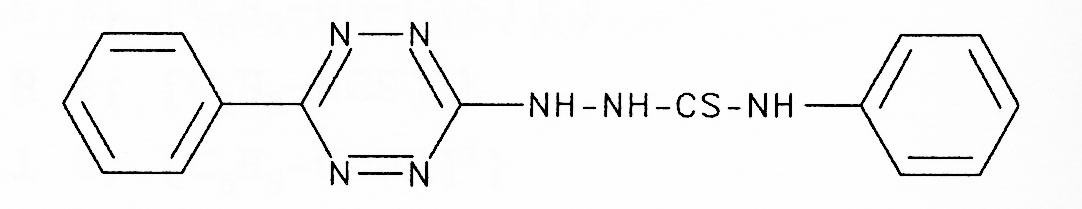
Analog wird mit Phenylisothiocyanat das entsprechende Thiosemicarbazid erhalten.
Fp.: 198 °C Ausbeute: 79%
Reaktion von Hydrazino-1,2,4,5-tetrazinen mit Thiophosgen
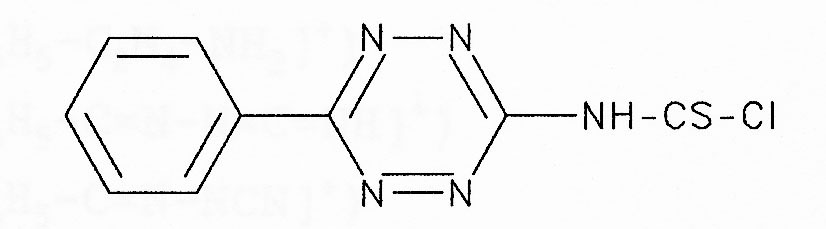
Die Reaktion wir in Chloroform durchgeführt und verläuft quantitativ. Das N-(6-Phenyl-1,2,4,5-tetrazin-3-yl)-thiocarbamidsäurechlorid wird nach Abdestillieren des Chloroforms und des überschüssigem Thiophosgens in Chloroform gelöst und weiter umgesetzt.
N-substituierte Tetrazinyl-Thioharnstoffe
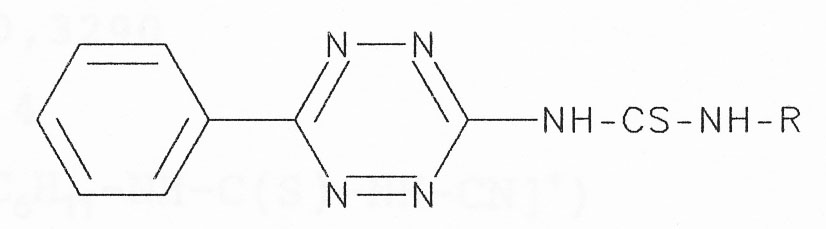
Das nicht isolierte Thiocarbamidsäurechlorid wird in der Chloroformlösung mit einem
Überschuss des Amins versetzt. Der Aminüberschuss wird mit verdünnter Salzsäure
ausgewaschen.
R = Phenyl Ausbeute: 43%
R = Cyclohexyl Ausbeute: 59%